Scientific journal
International Journal of Experimental Education
ISSN 2618–7159
ИФ РИНЦ = 0,827
ANIMAL MODEL «DIABETIC FOOT» ON THE BACKGROUND OF EXPERIMENTAL STREPTOZOTOCIN-INDUCED DIABETES
На сегодняшний день сахарный диабет является достаточно изученной патологией, существует множество лекарственных препаратов и современных схем терапии данного заболевания, однако, болезнь продолжает прогрессировать особенно в развитых странах [4]. По данным Всемирной Организации Здравоохранения, количество пациентов с диагностированным сахарным диабетом составляет около 160 млн., к 2025 г. прогнозируется удвоение количества пациентов с этим диагнозом. Следует отметить, что диабет является социально значимым заболеванием, поскольку сосудистые осложнения приводят к ранней инвалидизации пациентов и летальности [1, 3]. Одним из осложнений диабета является синдром «диабетической стопы». При данном состоянии наблюдается комплекс анатомо-функциональных изменений на фоне длительной гипергликемии, приводящей к развитию нейропатии, микро- и макроангиопатий, остеоартропатии, что приводит к повышенной травматизации и инфицированию мягких тканей стопы. В связи с чем, разработка мероприятий (в том числе фармакологической терапии), направленных на снижение возникновений осложнений при диабете является актуальной задачей.
Большое значение для определения вопросов патогенеза, клиники и терапии заболевания имеет экспериментальная диабетология. Экспериментальные модели диабета и его осложнений позволяют получить важные сведения не только для понимания патофизиологии заболевания, но и механизма антидиабетического действия лекарственных препаратов с целью их направленного применения [8, 10]. К настоящему времени разработан ряд моделей экспериментального диабета [11], основными из которых являются: хирургическая (полное или частичное удаление поджелудочной железы); химическая модель (используется введение химических веществ, избирательно воздействующих на b-клетки островков: аллоксан, стрептозотоцин), генетические модели (получение трансгенных животных). Моделирование «диабетической стопы», как правило, проводится на фоне стрептозотоцин-индуцированного диабета с принудительным инфицированием лапы Синегнойной палочкой (Pseudomonas aeruginosa) и Золотистым стафилококком (Staphylococcus aureus) [12, 13].
Целью данной работы стала разработка неинфекционной экспериментальной модели «диабетической стопы», с развитием ангио- и нейропатии.
Материалы и методы исследования
Исследование выполнено на 30 крысах-самцах популяции линии Wistar, полученных из питомника лабораторных животных РАМН «Рапполово».
Кормление животных осуществлялось стандартным полнорационным гранулированным комбикормом приготовленным по ГОСТ Р 50258–92. Доступ к воде и корму был свободный. Крыс-самцов содержали в поликарбонатных клетках по 5 особей, при температуре 20–22°С. Содержание животных осуществлялось в соответствии с Правилами надлежащей лабораторной практики (GLP) и Приказом Минздравсоцразвития РФ №708н от 23.09.2010 г. «Об утверждении правил лабораторной практики». Животные были разделены на контрольную (n=15) и опытную группы (n=15).
Формирование экспериментальной патологии у животных опытной группы проводили введением стрептозотоцина (Sigma, США) в дозе 60 мг/кг однократно внутрибрюшинно, спустя 15 минут после введения никотинамида (Sigma, США) в дозе 230 мг/кг (внутрибрюшинно).
С целью выявления биохимических и гистологических признаков диабета и его поздних осложнений у экспериментальных животных были проведены исследования в динамике. Концентрацию глюкозы в периферической крови измеряли глюкометром OneTouch Horizоn («Lifescan», США). Линейный диапазон измерения 1,1 – 33,3 ммоль/л. Гликозилированный гемоглобин (HbA1c) в крови определяли с использованием набора «Диабет-тест» (Фосфосорб, Россия). Метод основан на аффинной хроматографии гликозилированной и негликозилированной фракций гемоглобина в гемолизате крови. Линейный диапазон измерения 2,0 – 20,0 %. Подсчет ретикулоцитов проводился согласно унифицированной методике после их окраски готовым красителем – бриллиантовым крезиловым синим (Диахим-ГемиСтейн-РТЦ) в пробирке (суправитальный пробирочный метод).
Для гистологического и иммуногистохимического исследования материал фиксировали в 10 % растворе нейтрального формалина в течение 24 часов, и по общепринятой методике заливали в парафин [5]. Затем изготавливали срезы толщиной 5–7 мкм, которые окрашивали гематоксилином и эозином. Иммуногистохимическое исследование включало в себя определение экспрессии нейронального маркера PGP 9.5 с использованием моноклональных антител производства фирмы Abcam. Постановка реакции проводилась непрямым трехступенчатым иммуноферментным LSAB (Labeled streptavidin–Biotin, DakoCytomation, LSAB 2 System – HRP) методом визуализации; выявление пероксидазной активности осуществляли с помощью 3,3–диаминобензидина, препараты докрашивали гематоксилином Майера. Морфологическое исследование гистологических препаратов проводилось при помощи светооптического микроскопа CarlZeiss (Германия). Микрофотографирование проводили при помощи цифровой фотокамеры AxioScopeA1 (Германия).
Результаты исследования и их обсуждение
Как известно механизм действия стрептозотоцина связан с наличием в его химической структуре сахарозного остатка (гексозы), за счет которого, через транспортную систему ГЛЮТ-2, он включается β-клетками островков Лангерганса в обменные процессы вместо глюкозы. Попадая в клетку, стрептозотоцин разрушается с образованием свободных радикалов и NO·, в результате происходит алкилирование ядерной ДНК и гибель клетки [14]. Предварительное введение никотинамида приводит к снижению диабетогенного действия стрептозотоцина.
В ходе исследования было установлено, что спустя 5 недель у животных опытной группы наблюдали клинические проявления диабета, которые нашли отражение в статистически значимом увеличении концентрации глюкозы по отношению к контрольным животным более чем в 4 раза (рис. 1).
К концу исследования (14 неделя) у животных опытной группы сохранялась гипергликемия, которая дополнительно сопровождалась статистически значимым увеличением концентрации гликозилированного гемоглобина (HbA1c) более чем в 2 раза (7,4±0,1 %). Увеличение концентрации HbA1c характерно для течения гипергликемии, длительность имеет положительную корреляцию с частотой развития осложнений при диабете. Данный показатель отражает риск развития осложнений диабета.
Спустя 10 и 14 недель после моделирования экспериментального стрептозотоцин-индуцированного диабета у животных опытной группы наблюдали статистически значимое увеличение уровня ретикулоцитов более чем в 3 раза (табл. 1).
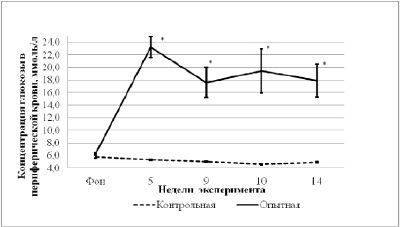
Рис. 1. Динамика изменения концентрации глюкозы в периферической крови крыс-самцов, ммоль/л
Таблица 1
Уровень ретикулоцитов в крови крыс-самцов, спустя 10 и 14 недель развития патологии, M±m (n=15)
|
Группа |
10 неделя |
14 неделя |
|
Ретикулоциты, ‰ |
Ретикулоциты, ‰ |
|
|
Контрольная |
15,5±1,4 |
14,2±1,7 |
|
Опытная |
55,6±14,2* |
57,0±5,4* |
* – различия статистически значимы по сравнению с контрольной группой (р<0,05).
На фоне хронического диабета в тканях возникает дефицит кислорода и компенсаторно происходит увеличение эритропоэза [6, 7], что сопровождается выходом в системный кровоток молодых эритроцитов и ретикулоцитов. Уровень ретикулоцитов в периферической крови при окислительном стрессе отражает степень гипоксии тканей [2, 9].
Гистологическая оценка подтвердила наличие изменений характерных для диабетической патологии. В опытной группе наблюдали типичные проявления микроангиопатии, характерные для отсроченных осложнений диабета (рис. 2–6). У животных данной группы наблюдали продуктивный капиллярит со слабо выраженным периваскулярным склерозом, а также склероз стенок артериол. В тканях выявляли периваскулярную лимфо-гистиоцитарную инфильтрацию от слабой до умеренной выраженности, частично затрагивающую периневральные зоны. Кроме того была выявлена аксональная дегенерация, демиелинизация и очаговый некробиоз аксонов. Трофические нарушения приводили к дистрофическими нарушениям в дерме, где отмечался выраженный гиперкератоз и слабо выраженный акантоз, местами с вовлечением в процесс придатков кожи (волосяных фолликулов, сальных и потовых желез). Патологический процесс частично затрагивал костно-суставную структуру в виде дистрофических изменений хрящевой ткани. В тканях крыс-самцов контрольной группы отличий от нормы не выявлено.
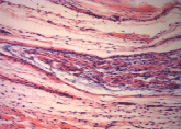
Рис. 2. Аксональная дегенерация и очаговый некробиоз аксонов в нервном стволе. Окраска гематоксилином и эозином. Увеличение 200
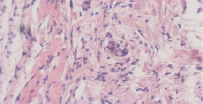
Рис. 3. Умеренно выраженная диффузная лимфоплазмоцитарная инфильтрация, преимущественно переваскулярных и переневральных зон, соединительнотканные «муфты» в переневральных зонах (стрелка). Увеличение 200
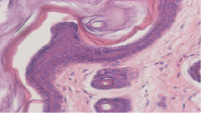
Рис. 4. Выраженный гиперкератоз и слабо выраженный акантоз, вовлечение в патологический процесс придатков кожи (волосяных фолликулов). Окраска гематоксилином и эозином. Увеличение 200
При иммуногистохимическом исследовании с применением маркера PGP 9.5 в опытной группе крыс-самцов наблюдали диабетическую нейропатию, которая выражалась в снижении плотности нервных волокон за счет аксональной дегенерации, демиелинизации и очагового некробиоза (рис. 5). В контрольной группе животных отличий от нормы не выявлено (рис. 6).
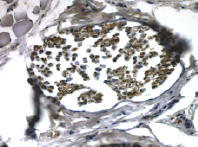
Рис. 5. Кожа стопы крысы контрольной группы. Нервные волокна без отклонения от нормы. Иммуногистохимическое окрашивание. Экспрессия нейронального маркера PGP 9.5 в осевых цилидрах. Увеличение 200
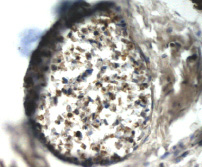
Рис. 6. Кожа стопы крысы опытной группы. Нервные волокна с очагами демиелинизации, дегенерации тигроидной субстанции осевых цилиндров. Иммуногистохимическое окрашивание. Снижение экспрессии нейронального маркера PGP 9.5 в осевых цилидрах. Увеличение 200
Таким образом, данные гистологического и иммуногистохимического исследования подтверждают развитие ангио- и нейропатий у лабораторных животных.
Выводы
Биохимические исследования крови лабораторных крыс-самцов с модельной патологией стрептозотоцин-индуцированного диабета выявили стойкие изменения углеводного обмена (гипергликемия (концентрация глюкозы в крови опытных животных находилась в диапазоне 17–23 ммоль/л), повышение концентрации HbA1 (в два раза по сравнению с контрольной группой)), увеличение уровня ретикулоцитов более чем в 3 раза, свидетельствующие о развитии диабета у животных.
Спустя 14 недель исследования у лабораторных животных определяются структурно-морфологические изменения, свидетельствующие о развитии ангио- и нейропатии.
Модель длительно-текущего стрептозотоцин-индуцированного диабета может быть рекомендована для изучения специфической активности новых препаратов, для терапии отсроченных осложнений диабета.
Библиографическая ссылка
Ковалева М.А., Макарова М.Н., Горячева М.А., Гущин Я.А., Макаров В.Г., Хомутников Е.А. МОДЕЛИРОВАНИЕ НА ЖИВОТНЫХ «ДИАБЕТИЧЕСКОЙ СТОПЫ» НА ФОНЕ ЭКСПЕРИМЕНТАЛЬНОГО СТРЕПТОЗОТОЦИН-ИНДУЦИРОВАННОГО ДИАБЕТА // Международный журнал экспериментального образования. 2016. № 7. С. 47-51;URL: https://expeducation.ru/en/article/view?id=10282 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/mjeo.10282

