Scientific journal
International Journal of Experimental Education
ISSN 2618–7159
ИФ РИНЦ = 0,827
MODIFIED EXPERIMENT ON ALUMINOTHERMY IN THE STUDENT CHEMISTRY MANUAL
При изучении энергетики химических процессов в курсе химии для бакалавров и специалистов технических специальностей предусмотрен лабораторный практикум. Обычно он включает колориметрические исследования процессов нейтрализации растворов кислот и оснований или изучение тепловых эффектов растворения кристаллогидратов и безводных солей [1]. Представляется целесообразным дополнить практикум работой по изучению тепловых эффектов алюминотермических процессов. Большая вариативность составов алюминий / оксид металла позволяет включить в работу элементы научного исследования [2]. Проведение работы после освоения лекционного материала и выполнения соответствующего домашнего задания позволит закрепить пройденный материал и выработать приемы его практического применения [3–5].
Восстановление металлов из их соединений более активными металлами при высокой температуре известно как металлотермия и относится к пирометаллургическим методам. Возможность осуществления процесса восстановления оксидов алюминием, протекающего по реакции
2/mMenOm + 4/3Al = 2n/mMe + 2/3Al2O3,
была впервые обоснована С. Девиллем в 1856 г. и получила широкое распространение после появления дешевых алюминиевых порошков. Величина энтальпии реакции алюминотермии ΔrH°298 в кДж может быть рассчитана по уравнению
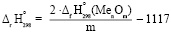 ,
,
где ΔfH°298(MenOm) – стандартная энтальпия образования оксида MenOm.
Энтальпия этой реакции зависит от используемого оксида, и для многих из них обеспечивает протекание процесса без подвода тепла извне. Газотермический эффект помимо используемого оксида определяется степенью измельчения и соотношением реагентов. Избыток алюминия повышает температуру и приводит к вспениванию и разбрызгиванию загрузки из-за испарения алюминия и воспламенения его паров. При традиционном осуществлении процесса в тигле, процесс самопроизвольно распространяется на всю шихту, вызывая расплавление металла и последующее разделение жидкого металла и шлака. При величине теплового эффекта процесса более 4600 кДж/кг продукта происходит существенное испарение алюминия и, часто, восстановленного металла, приводящее к выбросу продуктов реакции [3, 6], особенно при осуществлении процесса без тигля. Этот газодинамический эффект может быть использован для нанесения покрытия на подложку [7].
Сложность использования алюминотермии в лабораторном практикуме связана с высокими температурами в процессе эксперимента (более 2700 K), его пожароопасностью и отсутствием недорогих инструментов контроля параметров процесса, которые, ввиду их наглядности, могли бы быть использованы в студенческом практикуме. Поэтому при проведении реакции в тигле обычно исследуют остывшие продукты реакции после завершения синтеза [3]. Так как температура алюминотермического процесса превышает допустимые значения для термопар, а использование пирометра неинформативно из-за слоя шлака на поверхности и быстрого изменения температуры в зоне горения, не получается с очевидностью судить об энтальпии процесса и о влиянии на термохимические параметры различных добавок [8]. Требуется предложить безопасный и простой способ проведения синтеза, наглядно иллюстрирующий величину теплового эффекта реакции, а также равномерность протекания процесса. Важно, чтобы в распоряжении у студентов был такой материальный носитель, который можно легко анализировать простейшим способом.
По нашему мнению, перечисленным критериям отвечает проведение эксперимента в металлическом или керамическом реакторе цилиндрической формы с дном и крышкой с центральным расположением шихты и электроподжигом. Выбор оксидов должен обеспечивать протекание реакции с избыточной энтальпией таким образом, чтобы после инициирования процесса он протекал самопроизвольно с выбросом части продуктов в стороны от центра. Для их фиксации предназначена подложка, представляющая из себя свернутую в цилиндр полоску бумаги, холста, пластика, фольги и т.д., находящаяся внутри реактора вблизи его цилиндрической стенки. Реактор размещали в вытяжном шкафу для удаления газообразных продуктов реакции, закрывали негерметичной крышкой и дистанционно зажигали шихту. В результате опыта получали королек металла с шихтой в центральной части реактора и подложку с покрытием. Эти объекты полностью безопасны и могут быть исследованы студентами на своих рабочих местах.
Предложенная методика была реализована с оксидами, которые из-за большого теплового эффекта процесса обеспечивают расплавление и испарение восстановленного металла. Например, при использовании оксида железа (III) расчетное значение температуры процесса превышает 3134 К (температура кипения железа), что обеспечивает и расплавление, и испарение железа, а при использовании оксида железа (II) максимально достижимая расчетная температура равна 3038 К и испарения железа не происходит [9]. Таким образом, оксид железа (III) подходит для данной методики, а оксид железа (II) – нет. На практике наилучшее напыление получается при использовании смеси оксида меди (II) с алюминием [7]. Температура кипения алюминия 2792 К близка к температуре кипения меди 2840 К, энтальпия реакции составляет -1441 кДж/моль CuO, и эта смесь оптимально подходит для газотермического выброса продуктов на подложку. Использование оксида меди в качестве окислителя удобно также потому, что медь, полученная в результате восстановления оксида, не успевает окислиться за время нанесения на подложку. Слой меди красного цвета легко отличить на подложке от частиц оксида алюминия и иных оксидов. Также медь образует достаточно плотное покрытие с явной границей [7]. Для контроля степени восстановления оксида полезно использовать окрашенные оксиды, например оксид хрома (III) зеленого цвета, оксид молибдена (VI) желтого цвета. В случае оксида хрома (III), характеризующегося высокой температурой плавления, лимитирующей стадией является перенос восстановителя к поверхности оксида без заметной диффузии кислорода оксида, и восстановление протекает на поверхности частиц [10]. Газодинамический эффект обеспечивается парами алюминия, а в случае сходной температуры кипения также парами восстановленного металла. Пары алюминия в окислительной атмосфере подвергаются гомогенному горению [11], и на подложку попадает оксид алюминия. Состав королька металла может отличаться от состава покрытия на подложке, так как жидкий алюминий в тигле в меньшей степени подвержен воздействию атмосферы. В состав королька может входить как восстановленный из оксида металл, так и интерметаллиды алюминия [12, 13].
Для придания им огнестойкости горючие подложки были пропитаны раствором гидроортофосфата натрия, который при пиролизе катализирует процессы карбонизации за счет образования фосфорных кислот [14].
Материалы и методы исследования
Использовали порошковый алюминий ПА-4 основная фракция частиц 21–30 мкм, содержание основного вещества 98 %; и оксиды 99 % чистоты: оксид меди (II), оксид железа (III), оксид хрома (III), оксиды вольфрама и молибдена (VI). Алюминотермическая смесь содержала порошковый алюминий и один или несколько оксидов из перечисленных в близком к стехиометрическому соотношении.
Для выполнения работы группу разбивали на подгруппы из двух-четырех студентов, каждая из которых готовила шихту своего состава и проводила опыт с двумя подложками: пропитанной огнезащитным составом (5 % раствор гидроортофосфата натрия с высушиванием в сушильном шкафу) и непропитанной. Подложки в форме полуколец помещали в негерметичный реактор вблизи цилиндрических стенок, алюминотермическую смесь располагали в центре (рис. 1). Реактор помещали в вытяжной шкаф для удаления образующихся газообразных продуктов и поджигали смесь электроподжигом. Для завершения одного эксперимента требовалось около минуты, поэтому группа из 20–30 студентов работала с одним реактором, в котором подгруппы инициировали одну шихту за другой, заменяя подложки. Покрытие, полученное после завершения реакции, закрепляли на подложке лаком, разрезали подложку на фрагменты по числу студентов и изучали ширину полосы напыления, ее однородность, наличие термических повреждений подложки; сопоставляли полученные результаты с составом шихты и величиной энтальпии реакции.
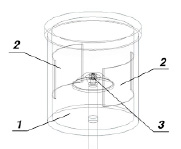
Рис. 1. Схема установки: 1 – цилиндрический реактор с дном и негерметичной крышкой, 2 – две симметрично расположенные подложки в виде полуколец, 3 – шихта с устройством электроподжига
Результаты исследования и их обсуждение
В результате опыта получали королек металла и подложку (полоса бумаги, картона, холста, пластмассы прямоугольной формы) с нанесенным на нее покрытием (рис. 2). Покрытие вдоль всей подложки имело наибольшую плотность в центральной части, ближе к периферии плотное покрытие переходило в двустороннюю кайму меньшей плотности. На периферии полосы находились симметричные участки без покрытия, часто содержащие небольшие локальные набрызги.
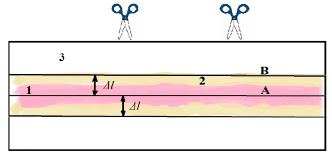
Рис. 2. Подложка после нанесения покрытия: А – срединная линия, В – линия, обозначающая границу напыления, 1 – центральная плотная часть покрытия, 2 – кайма с меньшей плотностью покрытия, 3 – участок подложки без покрытия. Обозначены линии разреза
Для обработки результатов эксперимента подложку разрезали на последовательные фрагменты по числу учащихся в подгруппе. Для каждого фрагмента проводили срединную линию и линию, обозначающую границу напыления и измеряли расстояние между ними Δl. Также фиксировали число и площадь периферийных набрызгов. При наличии прогаров фиксировали их число и площадь. Данные усредняли для каждой подгруппы. Затем сопоставляли полученные данные с составом шихты и строили график зависимости Δl от ΔrH0298 для всех составов шихты. Также для объяснения результатов использовали данные о температуре кипения металлов. Например, близость температур кипения алюминия и меди (расхождение в 48 К) обеспечивает отличное газотермическое напыление продуктов на подложку. Наличие металлической меди на подложке доказывает, что температура процесса превышала 2840 К. Легкое отделение шлака от расплава металла обусловлено также превышением плотности меди над плотностью алюминия в 3,31 раза. Замена части или всего оксида меди на оксид железа (III) несколько снижает газовыделение, ослабляя газотермический эффект, так как разность температур кипения алюминия и железа составляет 294 К. В этом случае масса навески должна быть достаточной для испарения железа. Наличие металлического железа на подложке означает, что температура процесса превышала температуру кипения железа 3134 К. Плотность железа превышает плотность алюминия в 2,9 раза, что обеспечивает разделение железа и шлака. Также было рассмотрено влияние на газотермическое напыление веществ, изменяющих вязкость шлака. Добавление 5 (мас. %) MoO3 приводило к значительному увеличению вязкости шлака. Выбросы становились локальными в виде редких четко очерченных пятен. На подложке было видно характерное для оксида молибдена (VI) желтое окрашивание. Это свидетельствует, что из-за повышенной вязкости, смесь не до конца восстанавливалась алюминием, и часть оксида молибдена испарялась и выбрасывалась на подложку. И температура плавления чистого оксида молибдена (VI) (1074 К), и температура кипения (1428 К), значительно меньше температуры кипения алюминия, так что причина повышения вязкости, видимо, связана с образованием оксидом молибдена (VI) комплексных соединений [15]. Добавление фторалюмината натрия, наоборот, делало распределение продуктов на подложке более равномерным.
Интересный эффект наблюдался при добавлении к смеси оксида хрома (III), который обладает высокой температурой плавления и кипения (2708 и 4273 К соответственно). Так как температура кипения алюминия лишь на 74 К превышает температуру плавления оксида хрома (III), в восстановлении такой смеси основную роль играет перенос восстановителя к поверхности оксида. Время контакта реагентов мало, а из-за отсутствия диффузии кислорода в оксиде процесс протекает в тонком приграничном слое, и оксид хрома восстанавливается лишь частично. Поэтому на подложке присутствует значительное количество невосстановленного оксида хрома (III), имеющего характерный зеленый цвет. Для получения более заметного газодинамического эффекта в этом случае использовали смесь оксидов меди (II) и хрома (III).
Использование подложек из горючего материала позволяет продемонстрировать влияние огнезащитной пропитки на устойчивость бумаги, картона или холста к высокотемпературному воздействию. Для пропитки не подходят составы, увеличивающие объем при разложении, например силикатные системы с карбонатом калия, мешающие закреплению покрытия на подложке. По этой же причине не использовали соли аммония. Оптимальным материалом для пропитки подложки оказался гидроортофосфат натрия, который после пропитывания 5 %-ным раствором и высушивания не мешал нанесению покрытия.
Заключение
Показана возможность проведения лабораторной работы по термохимии с использованием алюминотермических реакций и фиксацией части продуктов на подложке газотермическим напылением. Газотермическое напыление продуктов на доступные подложки позволяет удобно и наглядно продемонстрировать особенности протекания процесса, сопоставить термодинамические характеристики с результатами реакции. Наиболее удобна для этих целей смесь алюминия с оксидом меди (II), дающая покрытие из металлической меди характерного красного цвета. Добавление к смеси оксида молибдена (VI) желтого цвета повышает вязкость шлакового расплава, что приводит к неоднородным выбросам на подложку. Добавление оксида хрома (III) зеленого цвета, имеющего высокую температуру плавления, удобно демонстрирует более медленное восстановление, лимитированное диффузией алюминия к поверхности оксида. Одновременное помещение в реактор подложек из акварельной бумаги, холста и картона без пропитки и с огнезащитной пропиткой позволяет изучить огнезащитное действие гидроортофосфата как катализатора карбонизации.
Библиографическая ссылка
Богословский С.Ю., Кузнецов Н.Н., Атангулова А.Д. МОДИФИЦИРОВАННЫЙ ЭКСПЕРИМЕНТ ПО АЛЮМИНОТЕРМИИ В СТУДЕНЧЕСКОМ ПРАКТИКУМЕ ПО ХИМИИ // Международный журнал экспериментального образования. 2023. № 2. С. 17-21;URL: https://expeducation.ru/en/article/view?id=12122 (дата обращения: 02.06.2026).
DOI: https://doi.org/10.17513/mjeo.12122

