Соединения со структурой шпинели на основе ферритов и хромитов переходных элементов обладают сочетанием уникальных магнитных, электрических, оптических и других свойств, что обусловливает неослабевающий научный интерес к ним. Актуальной технологической задачей, открывающей перспективы широкого технического использования, вяляется поиск возможностей синтеза материалов, содержащих в одной подрешетке (октаэдрической или тетраэдрической) ионы металлов, способные образовывать катионы различной валентности. Присутствие разновалентных катионов в одной подрешетке связывают с проявлением высокой электропроводности (например, у магнетита [1]).
Структура шпинели представляет собой плотнейшую кубическую упаковку анионов кислорода, в которой 1/8 всех тетраэдрических и 1/2 октаэдрических позиций заняты катионами металлов. Элементарная ячейка шпинели представляет собой куб с удвоенным ребром: она состоит из 8 катионов А (в тетраэдрических позициях), 16 катионов В (в октаэдрических пустотах) и 32 анионов кислорода [2]. Формульная единица шпинели М2+М3+2 О4. Как правило, М2+ размещаются в А-узлах, М3+ – в В-узлах решетки шпинели (нормальная шпинель); при частичном или полном размещении М2+ в В-позициях структуру шпинели называют смешанной или обращенной. Параметр обращенности λ – количество катионов Ме3+ , занимающих тетраэдрические позиции решетки.
Синтез твердых растворов шпинельного типа на основе хромитов переходных элементов обычно сопряжен с большими энергетическими и временными затратами [2], проходит при высоких температурах [3] и часто требует использования специальной аппаратуры. Целью исследования являлось изучение технологических особенностей и процессов образования фаз в системе FeO-NiO-Fe2O3-Cr2O3.
Образцы ферритов-хромитов никеля-железа были получены по керамической технологии из оксидов никеля (II), железа (III), хрома (III) марки хч, оксалата железа (II), в соотношении FeO-Cr2O3 (образец 1) и 0.75 (FeO-Cr2O3) – 0.25 (NiO-Fe2O3) (образец 2). Для интенсификации процессов фазообразования в смесь исходных веществ вводили хлорид калия марки хч (до 1 % (масс.)) на стадии гомогенизации. Синтез проводили при температуре 900 оС в течение 5 часов. По окончании синтеза образцы отмывали от хлорида калия до отрицательной реакции на хлорид-ионы в фильтрате. Фазовый состав изучали на рентгеновском дифрактометре ДРОН-3, использовали Cо-Kα излучение.
Фазовый состав образца 1 представлен твердым раствором примерного состава (Fe0,33 Cr0,67)2O3 со структурой ильменита, рассчитанные параметры решетки образца: aг = 0,5002 нм, cг = 1,3634 нм.
В образце 2 присутствуют две фазы: 70 % – ильменит ((Fe0.33 Cr0.67)2O3) с параметрами решетки aг = 0,5007 нм, cг = 1,3628 нм., 30 % – твердый раствор примерного состава Ni0,83 FeII0,17 FeIII1,66 Cr0,34 O4 с параметром кубической ячейки a = 0,8304 нм. Параметр обращенности полученной шпинели λ ≈ 0,67 рассчитан с использованием понятия кластерных компонентов в соответствии с методикой, подробное описание которой приведено в [3]. На основании изучения строения электронных оболочек катионов [4] следует предположить, что Cr3+ и Ni2+ будут стремиться к размещению в октаэдрических узлах кристаллической решетки шпинели, ион Fe3+ – в тетраэдрических, для Fe3+ обе позиции эквивалентны. С учетом перечисленных факторов, распределение катионов можно представить следующим образом: FeIII0.67 FeII0.24 N0.09[Cr0.48 FeIII0.85 Ni0.67]O4. В этом случае все катионы Fe2+ и часть Fe3+ располагаются в тетраэдрической подрешетке шпинели, что может способствовать усилению обменного взаимодействия по типу
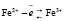
и благоприятствовать повышению электропроводности образцов.
При анализе полученных результатов следует отметить, что в рассматриваемых условиях не удается получить хромит железа (II) FeCr2O4. При синтезе в системе FeC2O4 – Cr2O3 образуется твердый раствор оксида железа (III) в оксиде хрома (III) со структурой ильменита. Полученные экспериментальные факты позволяют сделать вывод о том, что в образце 2 формирование феррита никеля (II) выступает стабилизирующим фактором образования шпинелеподобных структур и позволяет проводить синтез составов на основе Fe2+ .
Выводы
Изучены технологические особенности процесса фазообразования в смеси оксидов NiO – FeO – Fe2O3 – Cr2O3. Высказано предположение, что при формировании структуры шпинели в присутствии NiO удается стабилизировать получение образцов, содержащих катион Fe2+ . Предложена формульная единица формирующегося твердого раствора с распределением катионов по тетра- и октаэдрическим позициям решетки шпинели, согласно которой все катионы Fe2+ и часть Fe3+ располагаются в тетраэдрической подрешетке.

