В настоящее время ведущее место по степени отрицательного воздействия на окружающую среду занимают гальванические производства. Экологическая безопасность обусловлена тем, что гальваноотходы относятся ко 2-му и 3-му классам опасности. Они содержат ионы тяжелых металлов – железо, хром, свинец, медь, цинк, никель, марганец, кобальт, кадмий, оказывающих высокое токсичное, канцерогенное и мутагенное воздействие на живые организмы. Химические соединения металлов, например, их гидроксильные формы, присутствующие в шламах в значительных количествах, не трансформируются в инертные формы естественным путем. Они не устойчивы в кислой и щелочной средах и способны растворяться и мигрировать в почву и воду.
Вместе с тем, при использовании эффективного способа переработки, гальваношламы могут служить источником получения ценных компонентов, таких как металлов и их соединений. Кроме того, существует еще и экономический аспект проблемы утилизации тяжелых металлов, т.к. ежегодно в мире накапливается огромное количество шлама гальванических производств, потери цветных металлов исчисляются сотнями тысяч тонн. Одним из таких методов является ионный обмен.
В практике все большее применение находят природные минеральные сорбенты. В качестве минеральных сорбентов все чаще используют горные породы и минералы, обладающие способностью извлекать из водных систем токсичные примеси, в том числе и тяжелые металлы. Поэтому задача разработки экономически эффективных и экологически безопасных способов очистки сточных вод гальванических производств является актуальной.
Целью настоящей работы является изучение сорбционной активности монтмориллонита (ММТ) по отношению к ионам марганца и никеля.
Процесс ионного обмена на пористых сорбентах является сложным и многостадийным процессом. На сорбционную способность ММТ влияет природа их обменного комплекса. В результате замены одних ионов на другие можно изменять свойства поверхности ММТ.
Монтмориллонит представляет собой природный полимер. Кристаллическая решетка ММТ представляет собой трехслойный пакет, в котором октаэдрический слой с центральным атомом алюминия совмещен с двумя внешними кремнекислородными тетраэдрическими слоями. Внутри частиц ММТ увеличен электростатический дисбаланс, результатом чего является повышение отрицательного заряда на поверхности, который компенсируется адсорбцией катионов Na+, Ca+ и других щелочных металлов. Толщина пластин монтмориллонита составляет примерно 1 нм, тогда как поперечный размер находиться в диапазоне от нескольких нанометров до нескольких микрон. Благодаря такой «плоской» форме частиц ММТ возможно создание материалов, в которых пластинки ММТ располагаются друг над другом образуя высоко текстурированные слои в полимерной матрице.
О сорбционных свойствах ММТ можно судить по изотермам, характеризующим зависимость сорбционной способности ММТ от концентрации в растворе ионов марганца и никеля. Количественная адсорбция (Г) определяется избытком ионов на границе фаз по сравнению с равновесным количеством данных ионов в растворе. Экспериментально величину адсорбции ионов марганца и никеля вычисляли по уравнению:
 ,
,
где Cисх – исходная концентрация ионов марганца и никеля в растворе, ммоль/л; Сравн – равновесная концентрация ионов марганца и никеля, ммоль/л; Vр-ра – объем раствора, л; mсорбента – масса сорбента (ММТ), г.
Изотермы, полученные при сорбции ионов марганца и никеля на природном сорбенте ММТ, по внешнему виду похожи и напоминают изотерму смешанной структурой [1]. С увеличением концентрации исходного раствора степень извлечения ионов Mn2+ и Ni2+ из растворов уменьшается. Степень очистки растворов определяли по формуле
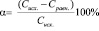 ,
,
где Cисх – исходная концентрация ионов марганца и никеля в растворе, мг/л; Сравн – равновесная концентрация ионов марганца и никеля в растворах после процесса сорбции, мг/л.
При образовании исходных растворов нитратов меди и цинка возможно протекание гидратообразования с выделением плохо растворимых гидроксидов Mn(OH)2 и Ni(ON)2, а также гидролиз катионов марганца и никеля. Оба эффекта способны оказывать влияние на результаты сорбции. В 1М растворах начальная величина водородного показателя среды при начале гидратообразования pHгидр для Mn2+ равна 7,8 и для Ni2+ – 6,7 [2], в случае 0,01М растворов Mn2+ и Ni2+ соответственно 8,8 и 7,7 [2], а при полном осаждении, где автор принимает концентрацию 10–5 М, pHгидр составляет 10,4 и 9,5 [2].
В связи со снижением в процессе сорбции концентраций Mn2+ и Ni2+, гидролизующихся по уравнению
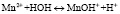 ,
,
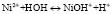 ,
,
происходит непрерывное изменение водородного показателя среды. Величина рН может быть рассчитана из зависимости (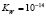 )
)
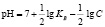 ,
,
где 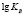 и С – соответственно константа диссоциации слабого основания, образующего соль по второй ступени, равная для Mn(OH)2 (5⋅10–4) Ni(OH)2 (2,5⋅10–5) [2]. Результаты расчетов показали, что по мере снижения содержания ионов Mn2+ и Ni2+ рН раствора существенно возрастает. Эти данные подтверждают и экспериментальные измерения рН растворов после сорбции ионов.
и С – соответственно константа диссоциации слабого основания, образующего соль по второй ступени, равная для Mn(OH)2 (5⋅10–4) Ni(OH)2 (2,5⋅10–5) [2]. Результаты расчетов показали, что по мере снижения содержания ионов Mn2+ и Ni2+ рН раствора существенно возрастает. Эти данные подтверждают и экспериментальные измерения рН растворов после сорбции ионов.
Глубина сорбционного извлечения марганца и никеля из сточных вод определяется большим количеством факторов, которые легко регулируются при технологической реализации процесса. К этим факторам можно отнести удельную массу сорбента, предварительную его подготовку (перевод в солевую форму), рН растворов, линейную скорость потока. Особое значение имеет высота слоя сорбента и его фракционный состав.
В заключении следует отметить, что исследуемый сорбент природный монтмориллонит по величине обменной емкости близок к синтетическим органическим катионитам. Это позволяет использовать данный сорбент для очистки сточных вод от тяжелых элементов.
Библиографическая ссылка
Пимнева Л.А., Королева М.Н. СОРБЦИОННАЯ ОЧИСТКА ПРОМЫШЛЕННЫХ СТОЧНЫХ ВОД ОТ ИОНОВ МАРГАНЦА И НИКЕЛЯ // Международный журнал экспериментального образования. 2015. № 3-1. С. 83-84;URL: https://expeducation.ru/ru/article/view?id=6705 (дата обращения: 15.04.2026).

